코넬대 의생명공학과 일라나 브리토(Ilana Brito)교수는 "누가 누구와 유전자를 교환하는지 알아낼 수 있다면 이것이 실제로 어떻게 발생하는지에 대한 통찰력을 제공하고 이러한 프로세스를 제어할 수 있을 것"...
유전자는 태어날 때만 유전되는 것이 아니다. 박테리아는 항생제 내성 확산의 주요 원인인 수평적 유전자 전달(horizontal gene transfer)이라는 과정을 통해 서로에게 유전자를 전달하거나 환경에서 선택하는 능력을 가지고 있다고 한다.
코넬대학교(Cornell University) 연구팀은 인공지능(AI) 머신러닝을 사용하여 기능별로 유기체를 분류하고 이 정보를 사용하여 유전자가 유기체 간에 어떻게 전달되는지를 거의 완벽에 가까운 정확도로 예측했다.
이는 잠재적으로 항생제 내성(antibiotic resistance)의 확산을 막는 데 사용할 수 있는 매우 중요한 접근 방식이다.
이 연구를 주도한 코넬대 의생명공학과 일라나 브리토(Ilana Brito)교수는 "유기체는 기본적으로 다른 유기체로부터 내성 유전자를 획득할 수 있습니다. 따라서 박테리아가 어떤 유기체와 교환 하는지 알면 도움이 될 뿐만 아니라 이러한 전달에 유기체를 연루시키는 추진 요인이 무엇인지 알아낼 수 있습니다"라고 말했다.
이어 그는 "누가 누구와 유전자를 교환하는지 알아낼 수 있다면 이것이 실제로 어떻게 발생하는지에 대한 통찰력을 제공하고 이러한 프로세스를 제어할 수 있을 것입니다"라고 덧붙였다.
많은 새로운 형질이 유전자 전달을 통해 공유된다. 그러나 과학자들은 일부 박테리아가 유전자 전달에 관여하는 반면 다른 박테리아는 그렇지 않은 이유를 밝혀내지 못했다.
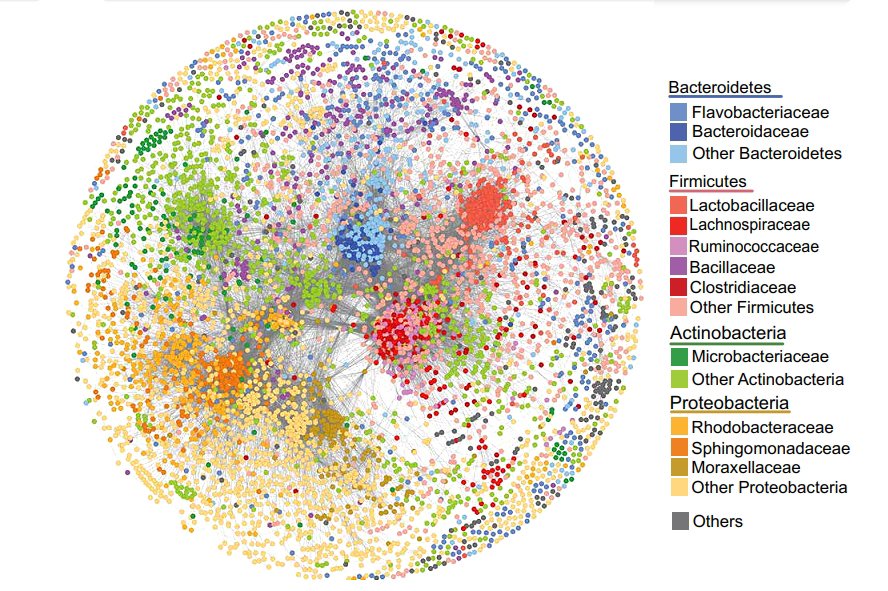
연구팀은 개별 가설을 테스트하는 대신 박테리아 게놈과 DNA 복제에서 탄수화물 대사에 이르기까지 다양한 기능을 조사하여 "누가"가 유전자를 교환하고 이러한 교환 네트워크를 주도했는지 식별한 것이다.
또한 여러 머신러닝 모델을 사용했으며, 각 모델은 데이터에 포함된 다양한 현상을 보여주었다. 이를 통해 그들은 동일한 유기체의 균주에 걸쳐 서로 다른 항생제 내성 유전자의 다중 네트워크를 식별할 수 있었다.
이 연구를 위해 연구팀은 토양, 식물, 바다와 관련된 유기체에 초점을 맞추고 있지만, 이 AI 모델은 매년 수천명의 사람들의 생명을 앗아가는 저항력이 강한 박테리아 아시네토박터 바우마니(Acineobacter baumannii)와 대장균(Escherichia coli)과 같은 병원균과 개인의 장 마이크로바이옴과 같은 국소적인 환경 내에서도 잘 식별된다. 또 모델은 항생제 내성 유전자에 적용될 때 특히 효과적이라는 것을 발견했다.
여기서, 가장 큰 시사점 중 하나는 특히 항생제 내성에 대한 박테리아 유전자 교환 네트워크가 예측 가능하다는 것이며, 데이터를 보면 이해할 수 있고, 실제로 각 유기체의 게놈을 보면 더 잘 알 수 있었다고 한다.
또한 가장 놀라운 발견 중 하나는 모델링이 아직 관찰되지 않은 인간 관련 박테리아와 병원체 사이의 가능한 많은 항생제 내성 전이를 예측했다는 것이다.

브리토 교수는 "이 유전자가 어떻게 퍼지는지 예측할 수 있다면 환자의 장에서 관찰되는 내용에 따라 특정 항생제를 선택하거나 개입할 수 있다고 상상할 수 있습니다"라고 강조했다.
이어 그는 "더 광범위하게, 우리는 특정 유형의 유기체가 특정 환경에서 다른 유기체와 함께 이동할 것으로 예측되는 위치를 볼 수 있습니다"라며, "그리고 이 데이터에 새로운 항생제 표적이 있을 수 있다고 생각합니다"라고 덧붙였다.
한편, 이 연구 결과는 사이언스 어드밴시스(Science Advances)에 '수평적 유전자 이동과 항생제 내성의 출현을 예측하는 기능(Functions Predict Horizontal Gene Transfer and Emergence of Antibiotic Resistance-다운)'란 제목으로 22일(현지시간) 게재되었다.

